非酒精性脂肪性肝炎(Nonalcoholic Steatohepatitis,以下简称NASH),是非酒精性脂肪性肝病(NAFLD)疾病谱中的一个重要发展阶段,具有以下特点:
流行广,患者群体大
NASH全球流行率在1.5-6.45%[1]。非酒精性脂肪肝(NAFL)群体中约30%会发展为NASH。
疾病向年轻化发展
人们生活习惯的改变(喜爱高糖高脂饮食、缺乏运动等)及肥胖在青少年中比例增加,预计NASH流行率及患病率将会继续增加,并向年轻化发展。
预后不良风险激增
表现NASH及肝脏纤维化症状的患者群体整体死亡率、肝脏特异性病死率等大幅升高。在美国,NASH是肝细胞肝癌的最常见病因,也被视作肝移植需求的指向标[2]。
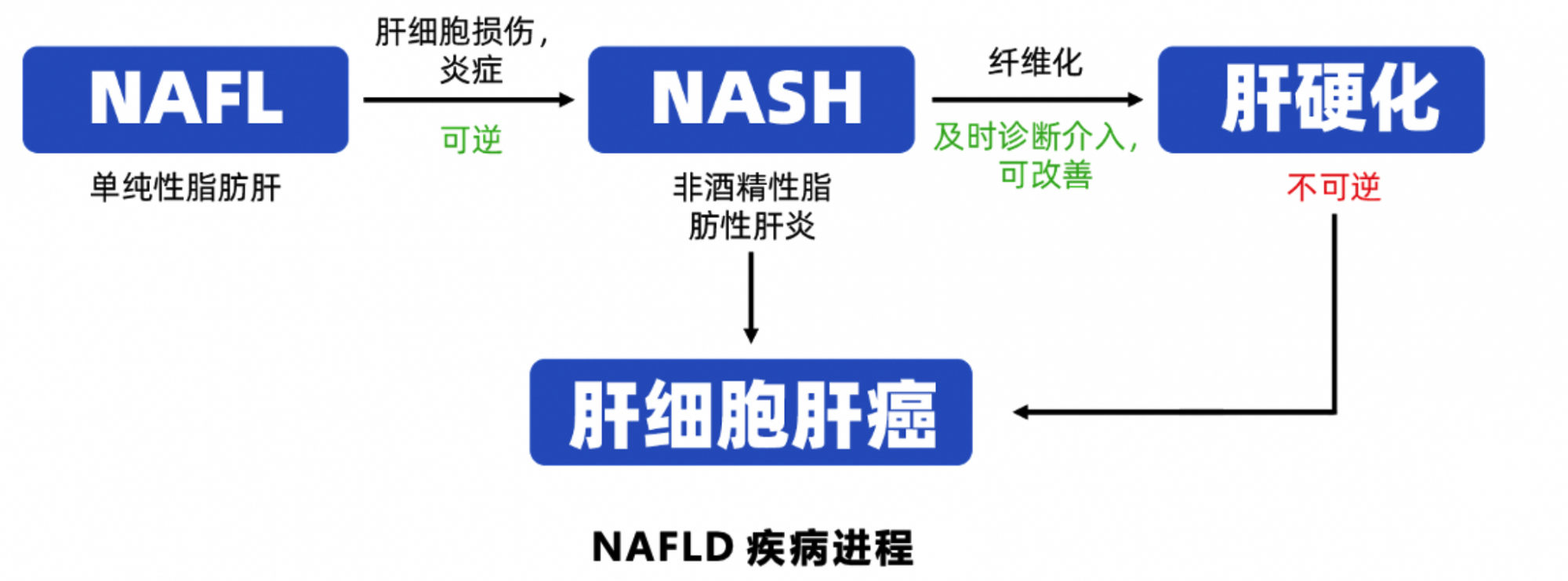
由此可以看出,NASH在NAFLD进程中是非常关键的临床介入节点。及时诊断及治疗有助于识别肝硬化、癌症和慢性肝病致死等风险,提升患者生命质量。
NASH的特征性病变主要体现在病理组织学上,肝脏需同时表现肝细胞脂肪变性、气球样变性和炎症。
肝脏活检作为FDA对于NAFLD唯一认证的金标准,在临床上常用于NASH诊断。评价标准主要包括NAS (NAFLD activity score) 和SAF (steatosis activity fibrosis),其中NAS应用范围更加广泛。
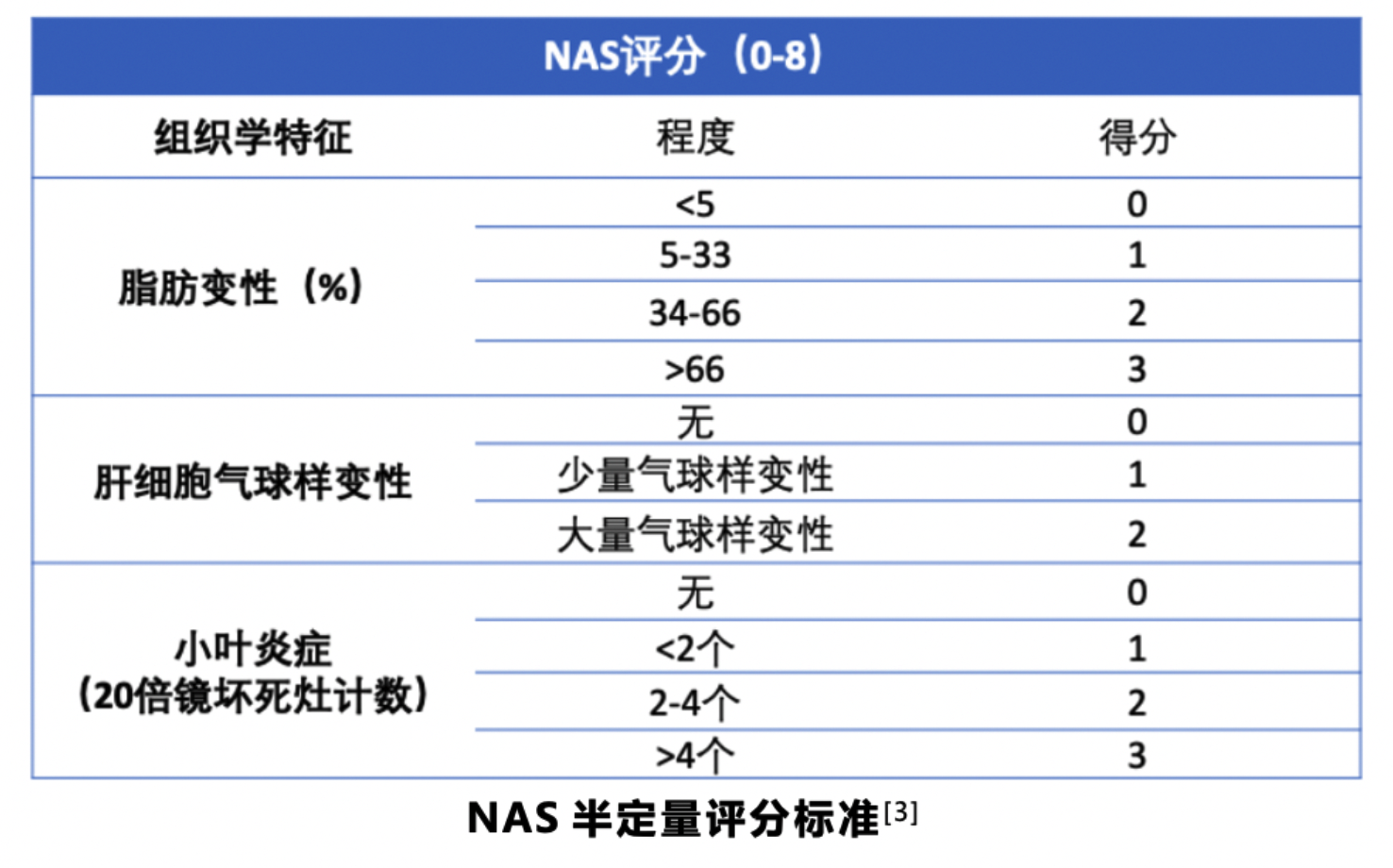
NAS系统包括14项组织学特征,其中4项为半定量指标:

因纤维化通常被认为是疾病活动的结果且不可逆,因此与其他三项分开评分,另外9项以是否存在为结果。
NAS>=5与NASH诊断相关性强,NAS<3则不是“NASH”。
面对这一棘手的全球公共卫生难题,市面上尚无已获批的直接治疗药物,国际上也没有统一的应对战略指导。
对于科研人员和临床医生来说,还有很多前期探索工作需要进行。选择合适的动物模型进行临床前体内研究,不仅可以大大缩短成模时间,还能模拟人类患者的新陈代谢、病理组织学等特点,支持研究者探索NASH发病机制和新药/疗法的药效评估,加速前期研发。
维通利华推出饮食诱导NASH现货模型,可模拟NASH病理生理学和新陈代谢特点,节省研究者前期造模时间与精力,助力NAFLD疾病机制理解与新药评估研究。
经特殊饲料诱导后的小鼠,肝脏呈现NASH典型病理组织学特点:肝细胞脂肪变性,气球样变性和炎症。随着诱导时间增加,肝脏组织出现纤维化。

肝脏内出现不同程度的肝细胞脂肪变性,胞质中有大小不一的圆形空泡(黑色箭头);多见肝细胞气球样变性,细胞肿胀,核居中,胞质空泡化(红色箭头);多见淋巴细胞浸润(蓝色箭头)。随诱导时间增长,经天狼星红染色可见组织中有较多胶原纤维增生(纤维化)。
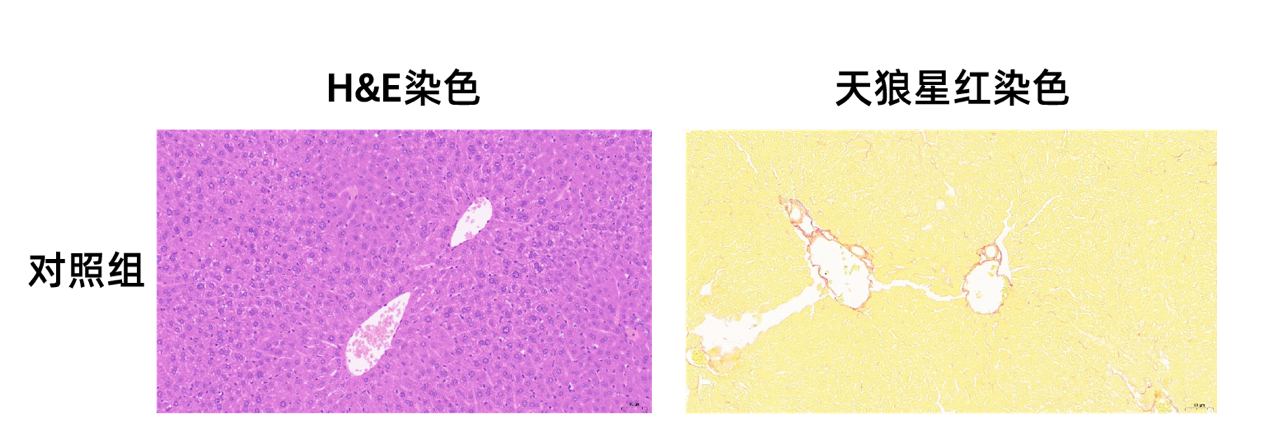
肝小叶中央静脉周围肝细胞和肝血窦呈放射状排列。肝脏细胞圆润饱满;肝板排列规则、整齐,肝窦无明显扩张或挤压;相邻肝小叶之间的门管区无明显异常;未见明显的炎性细胞浸润,无胶原纤维增生。
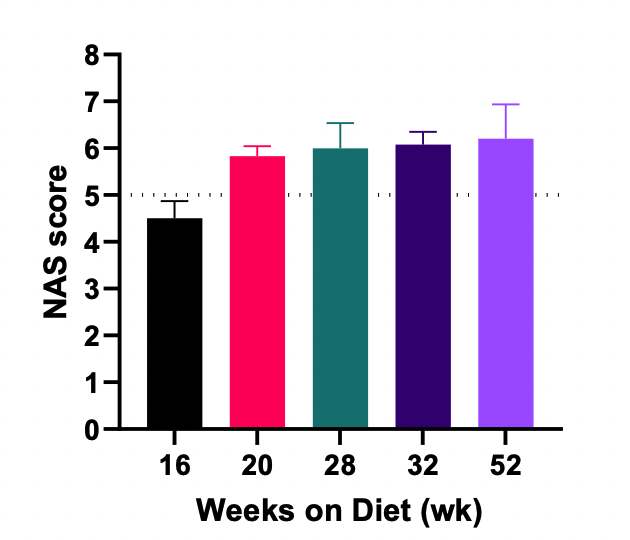
参考NAS对肝脏组织进行评分和判断。诱导至少20周后,NASH组平均分≥5,证明造模成功。
cGAS-STING通路作为先天免疫的重要组成部分,被激活后可能促成NAFL发展成NASH。
将特殊饲料诱导27周的NASH小鼠(维通利华提供)随机分为4组,按照组别分别给予生理盐水和不同剂量STING抑制剂,评估药物在小鼠体内的药效。
STING抑制剂可以通过抑制TBK1和p-TBK1的表达,减少IRF3磷酸化水平,降低p-TBK1/TBK1和 p-lRF3/IRF3的比值,来发挥其最终降低IFN-β表达的作用。随给药剂量增加,肝脏纤维化和炎症程度逐渐降低。体现了STING抑制剂对NASH有良好的剂量依赖性治疗作用。
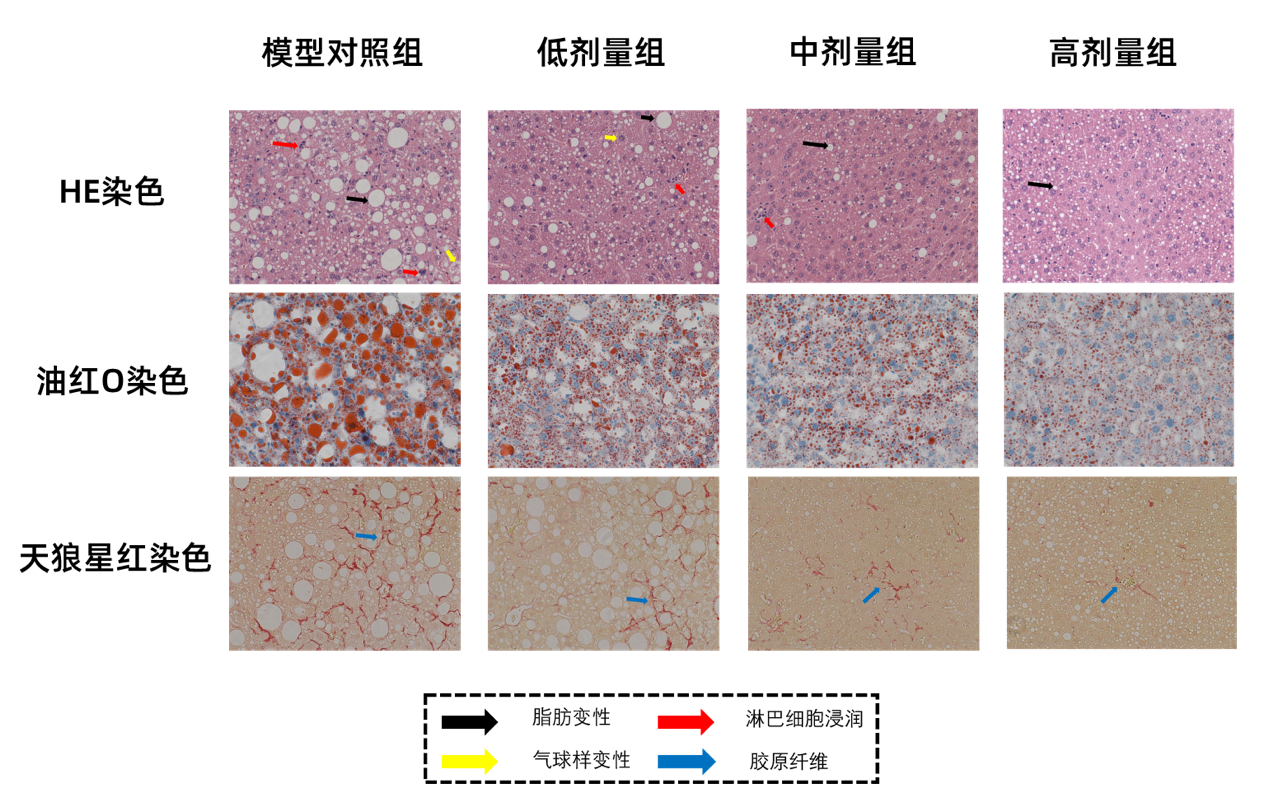
模型对照组肝脏呈现NASH典型病变且纤维化严重。随着给药剂量增加,肝细胞脂肪变性程度、炎性细胞浸润和纤维化等得到明显改善。
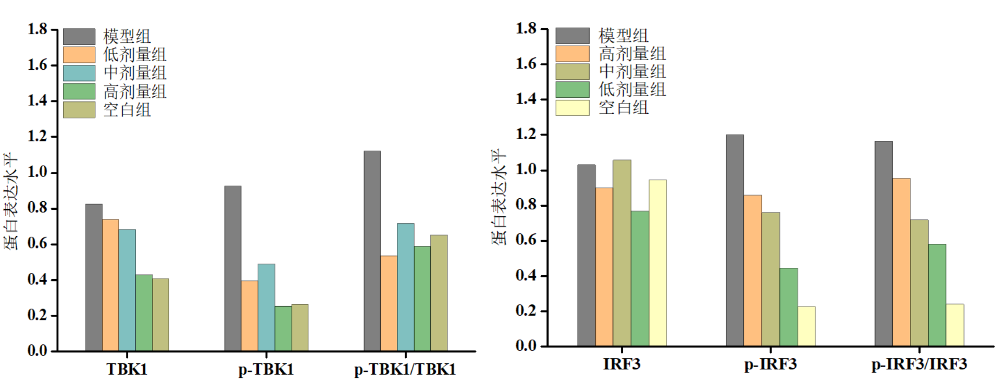
与模型对照组相比,STING抑制剂可显著下调TBK1、p-TBK1、和p-IRF3的表达,降低p-TBK1/TBK1和p-IRF3/IRF3的比值。
研究者反馈:维通利华NASH模型可高度模拟人类NASH病理组织学特点,在临床前研究中可以很好地支持药物药效学研究。
维通利华致力于让研究者获得高质量的动物模型,为此我们已在实验动物领域深耕20余年;除NASH模型外,我们还能够提供以下动物疾病模型:
老龄鼠(8-20月龄)-现货
饮食诱导肥胖模型(DIO)-现货
Ⅱ型糖尿病模型
动脉粥样硬化模型
高血压模型(SHR、盐敏感大鼠)
如果您想了解动物疾病模型的更多信息,可以咨询当地销售或者维通利华模型定制服务。
电话:010-8474 4522
邮箱:GEMS@criver.cn
非酒精性脂肪性肝病(Nonalcoholic Fatty Liver Disease, NAFLD)是指除酒精或其他明确损伤肝因素所致的,以弥漫性肝细胞大泡性脂肪病变为主要特征的一系列肝脏疾病谱。
按照组织病理学特征,NAFLD主要包括:
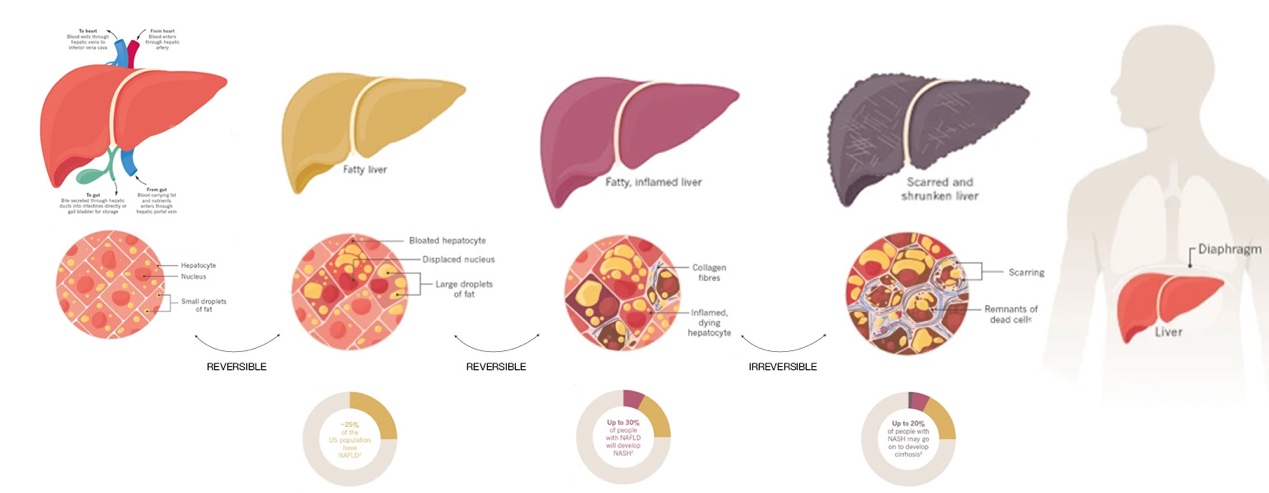
NAFL: 脂肪变性
脂肪在肝脏组织中堆积过多,导致肝细胞出现脂肪变性
NASH:脂肪变性、气球样变性、炎症
堆积过多的脂肪对肝细胞造成损伤,出现肝细胞气球样变性(即细胞结构损伤)和炎症
肝脏纤维化、肝硬化:
病程继续进行,胶原纤维替代坏死肝细胞填充组织,随着纤维化程度加重发展为肝硬化,肝脏功能几近衰竭,肝细胞癌(HCC)患病风险升高,需要肝脏移植。
随着人们生活习惯的改变,NAFLD已成为当代社会上最常见的肝脏疾病。据流行病学统计,NAFLD全球流行率高达25%,我国成年人患病率为29%。未来NAFLD仍呈现继续增长趋势[5]。预计到2030年,中国患病人群将增至3.14亿例,成为全球NAFLD患病率增长最多的地区[6]。
NAFLD也与肥胖、Ⅱ型糖尿病、高血脂症等代谢疾病高度相关,随着儿童肥胖呈现增长趋势,NAFLD也有年轻化发展趋势,青少年中流行率在0-3%[7]。因流行率与患病率日益增加,对患者和国家疾病负担加重,疾病机理尚不清楚、无直接治疗药物和统一疗法等特点,已成为代谢领域中的重点研究对象。
1.Wong RJ, Aguilar M, Cheung R, et al. Nonalcoholic steatohepatitis is the second leading etiology of liver disease among adults awaiting liver transplantation in the United States. Gastroenterology. 2015;148:547-555.
2.Anstee QM, Targher G, Day CP. Progression of NAFLD to diabetes mellitus, cardiovascular disease or cirrhosis. Nat Rev Gastroenterol Hepatol 2013;10:330–44. 10.1038/nrgastro.2013.41
3.Kleiner, David E et al. “Design and validation of a histological scoring system for nonalcoholic fatty liver disease.” Hepatology (Baltimore, Md.) vol. 41,6 (2005): 1313-21. doi:10.1002/hep.20701
4.Drew, L. Fighting the fatty liver. Nature 550, S102–S103 (2017).
5.ZhouF, ZhouJH, WangWX, et al. Unexpected rapid increase in the burden of NAFLD in China from 2008 to 2018: a systematic review and meta-analysis[J]. Hepatology, 2019, 70(4): 1119-1133. DOI: 10.1002/hep.30702.
6.Epidemiological Features of NAFLD From 1999 to 2018 in China. Hepatology. 2020 May;71(5):1851-1864. doi: 10.1002/hep.31150.
7.Zhang, Xin et al. “Increasing prevalence of NAFLD/NASH among children, adolescents and young adults from 1990 to 2017: a population-based observational study.” BMJ open vol. 11,5 e042843. 4 May. 2021, doi:10.1136/bmjopen-2020-042843




