肿瘤免疫高速发展的十年中,各种肿瘤免疫疗法都取得了较大突破,免疫检查点抑制剂,靶向T细胞的双特异性抗体,CAR-T细胞治疗等等,但这些疗法通常来说只针对一些血液瘤或者“热肿瘤”有效,对大部分实体瘤的疗效却差强人意。原因是在 “冷肿瘤”中几乎不存在免疫细胞,如何让免疫细胞浸润这些肿瘤从而发挥抗肿瘤活性是需要解决的难题。
近几年,如何逆转“冷肿瘤”,科学家及生物制药企业根据不同药物的原理,对应不同的患者设计出联合治疗。在近两年的AACR及ASCO会议上,我们越来越能意识到,联合疗法给患者带来的收益要远远大于单药。
2022年ASCO会议上,单单针对K药的联合疗法,高达十几项,均取得理想的效果。发表在2022年7月份Nature的文章 “Combination of T cell-redirecting bispecific antibody ERY974 and chemotherapy reciprocally enhances efficacy against non-inflamed tumours” 指出,采用GPC3/CD3双特异抗体ERY974和化疗联用的策略之后,成功的逆转了“冷肿瘤”,并在临床前研究中取得了较好的疗效。
目前靶点在T细胞上的肿瘤联合免疫疗法主要分为以下几类[1-3]:
(ICIs/BsAb):免疫检查点抑制剂/双特异抗体
huPBMC人源免疫系统重建模型具有制备周期短,成本低、高水平转化率的优势,被广泛应用于多种靶点在T细胞的肿瘤免疫药物研发中。huPBMC移植NOG小鼠会引起异种Xeno-GvHD反应,使得研究窗口期受限,无法满足组合疗法中更长研究窗口期的需求。
NOG-dKO小鼠,是指在NOG小鼠基础上敲除MHC I/II类分子的双敲模型。PBMC及CART等移植的T细胞无法识别小鼠的组织器官,从而无法进行免疫攻击,大大减缓了GvHD, 为研发者提供了充足的研发周期。
PBMC-NOG-dKO小鼠解决了PBMC移植后的窗口期问题,可以延长肿瘤免疫组合疗法的药效评估时间。
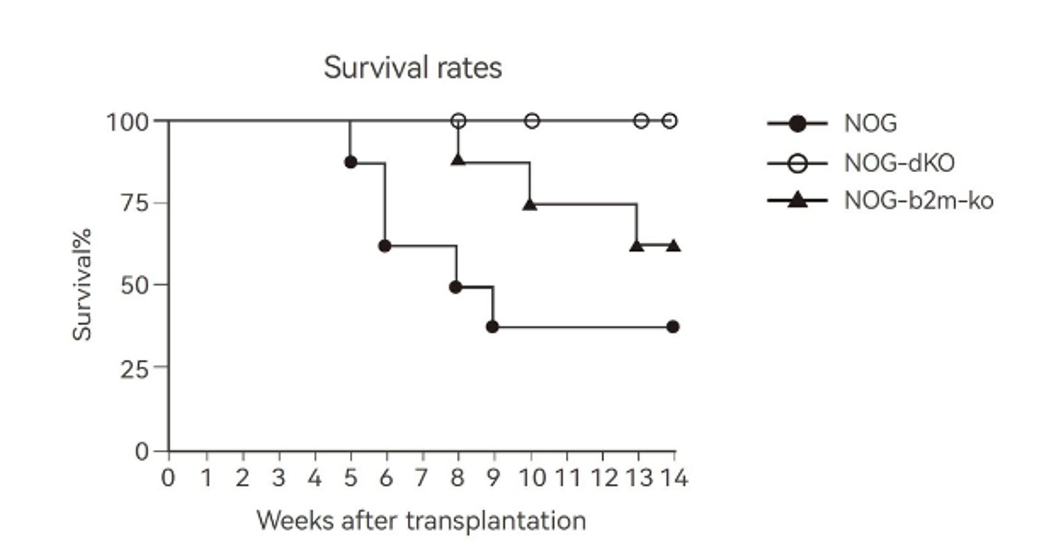
huPBMC-NOG-dKO小鼠可支持长时间的肿瘤负荷。
(人免疫细胞+人的肿瘤组织”的双人源化模型)
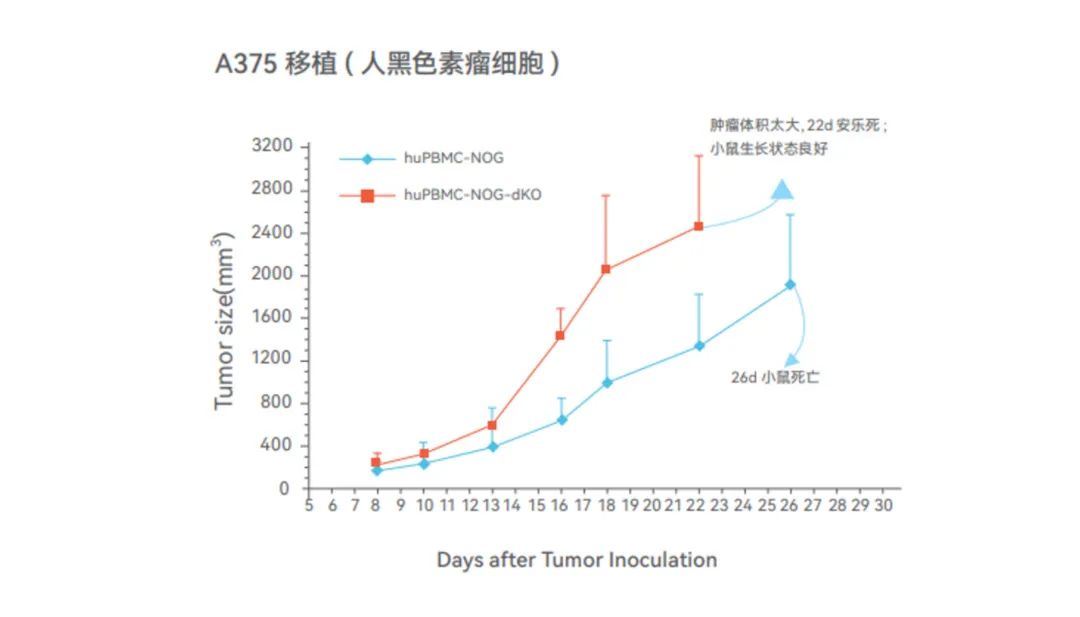
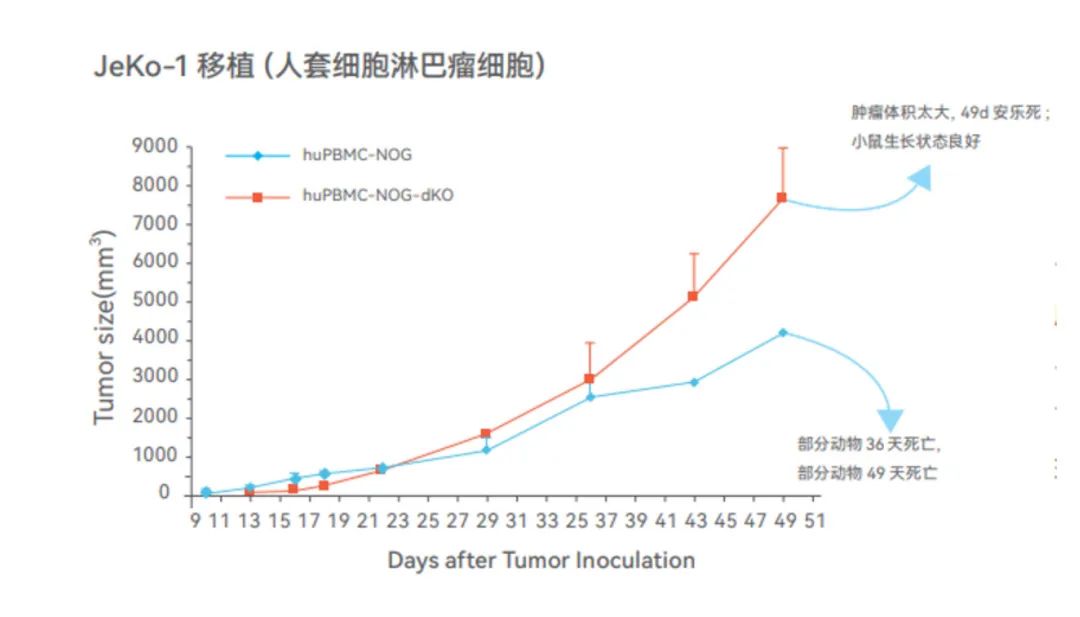
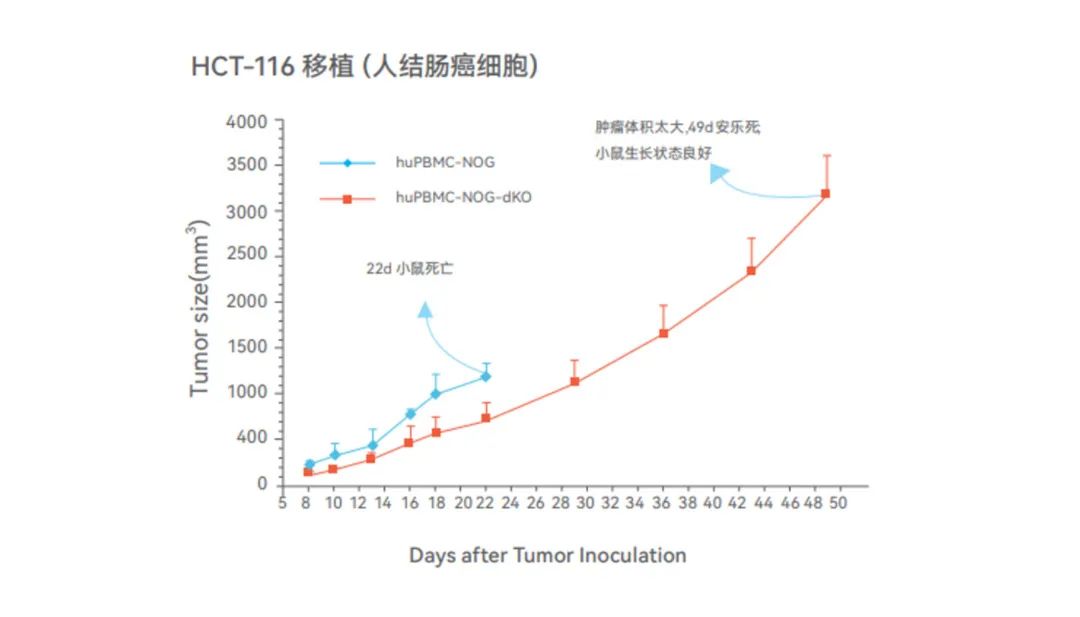
-NOG和NOG-dKO小鼠移植PBMC后均不会影响JeKo-1、A375、HCT-116等肿瘤的生长。
-NOG-dKO小鼠移植PBMC后,在肿瘤负荷的前提下,正常存活周期大于7周,而NOG小鼠会在3-6周出现死亡。
维通利华 Donor已验证的huPBMC-NOG-dKO小鼠, 丰富的HLA信息,hCD45信息,hCD4/hCD8信息,供研发者进行精准选择。

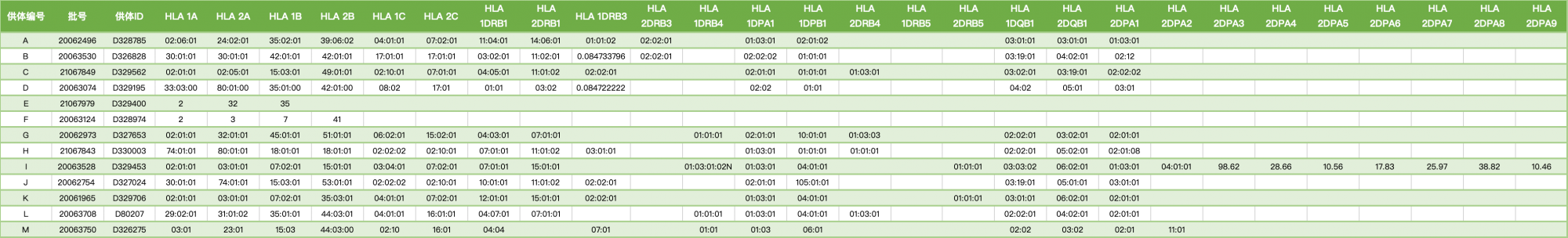
hCD45+(%)=hCD45+/(hCD45+mCD45)
hCD3+(%)=hCD3+/hCD45+
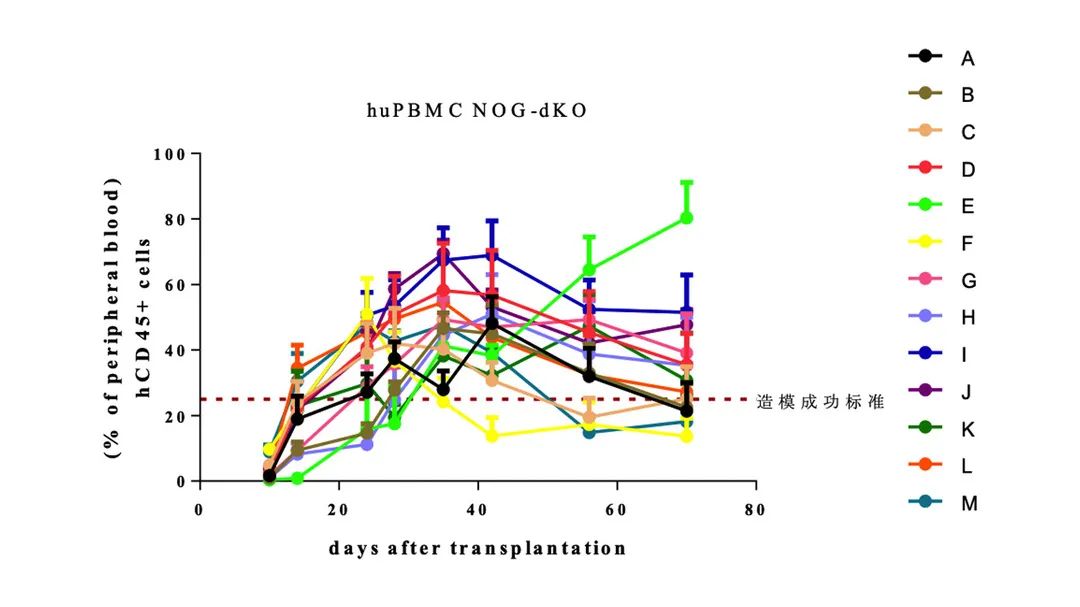
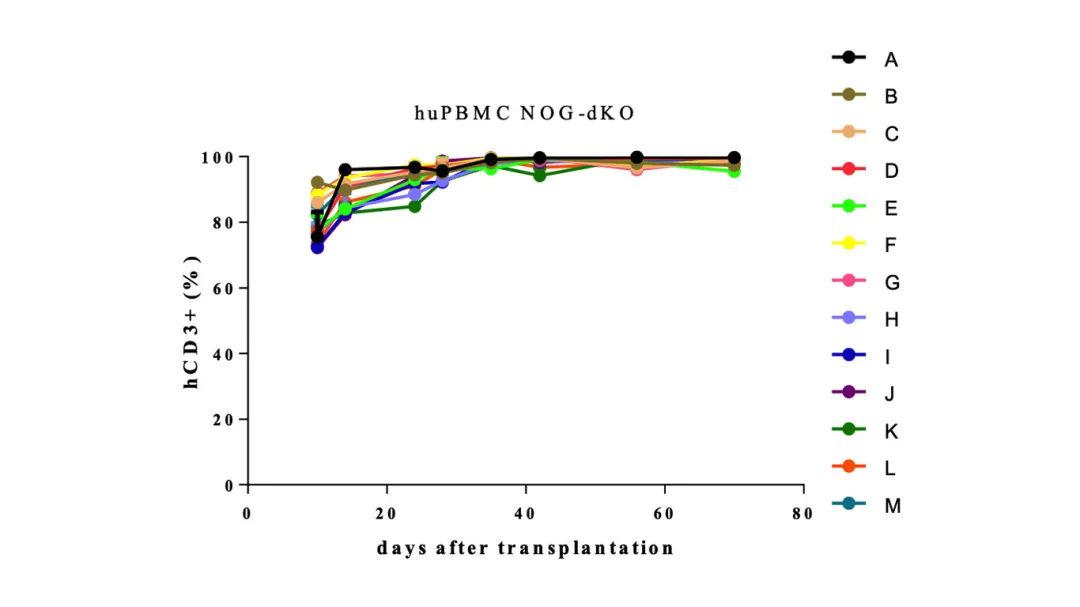
-13个供体均能比较好地重建人的免疫细胞(PBMC移植量为5M),重建效果均很理想,C,F,M供体移植8周后hCD45占比低于25%。
-huPBMC移植后3-8周时,hCD45+(%)重建水平一直处于高水平。
-重建的主要hCD3+T细胞,huPBMC移植3-4周后,hCD3+(%)比例高达99%。
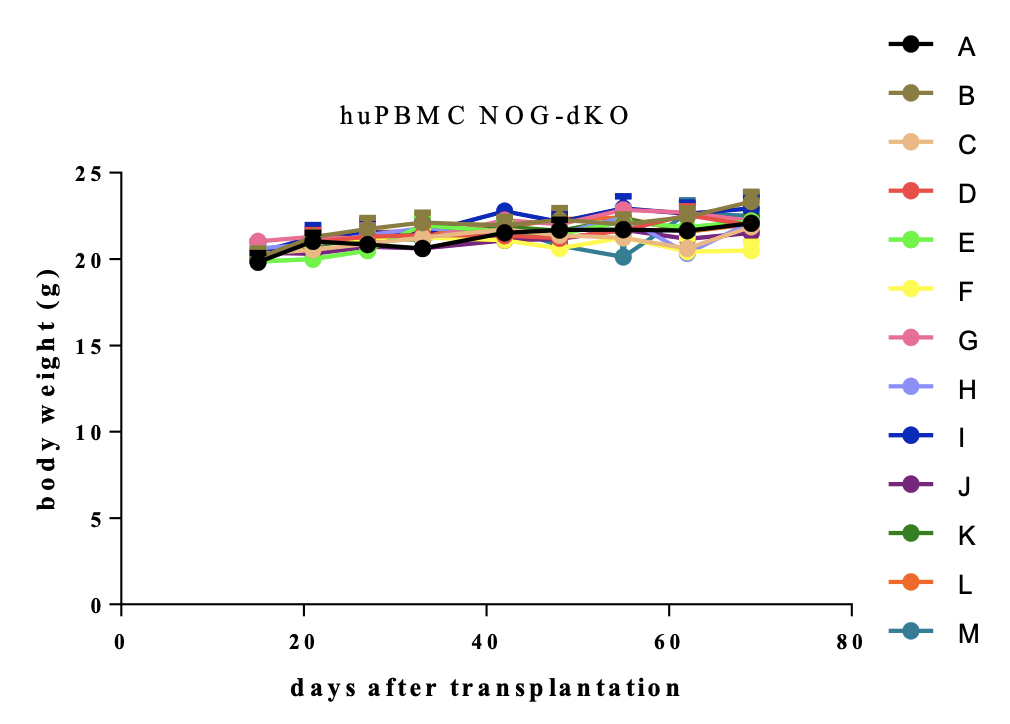
-NOG-dKO小鼠移植不同供体来源的PBMC后,小鼠体重稳步增长,无GvHD反应,可进行长期的研究窗口。
hCD4+(%)=hCD4+/hCD3+
hCD8+(%)=hCD8+/hCD3+
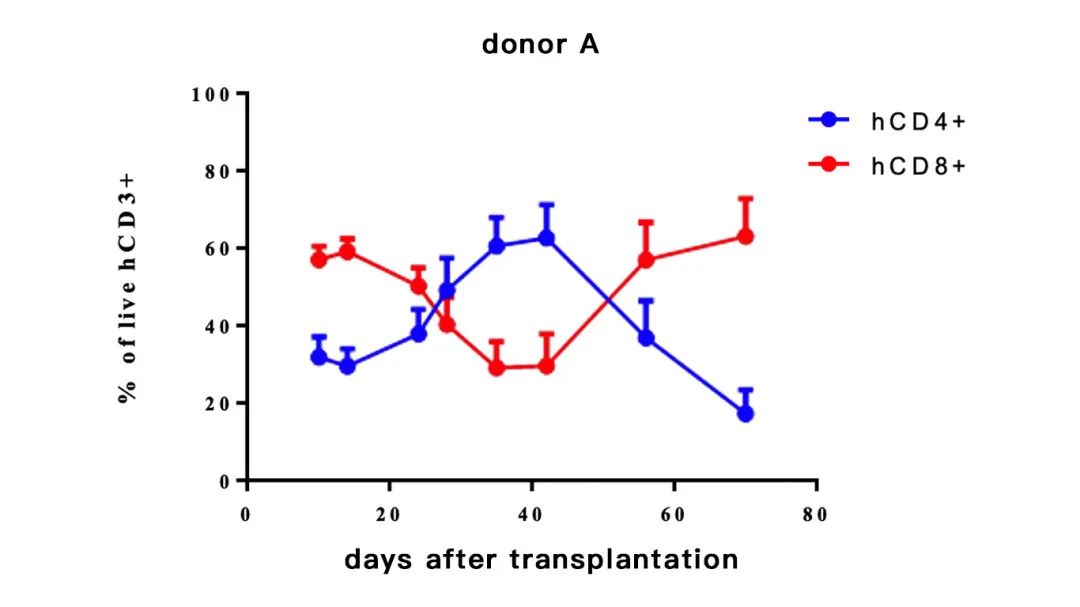
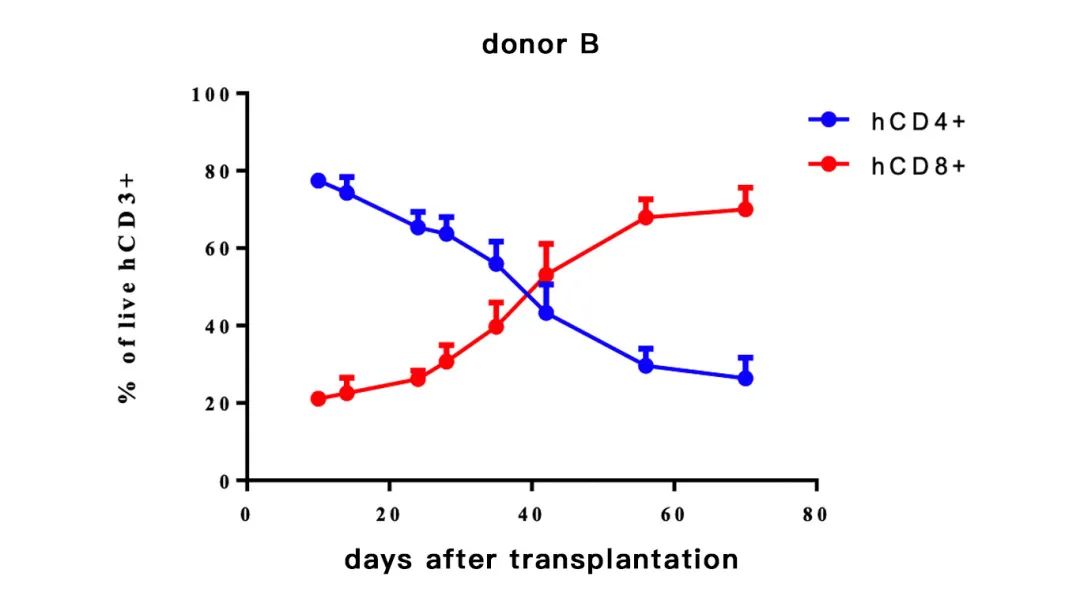
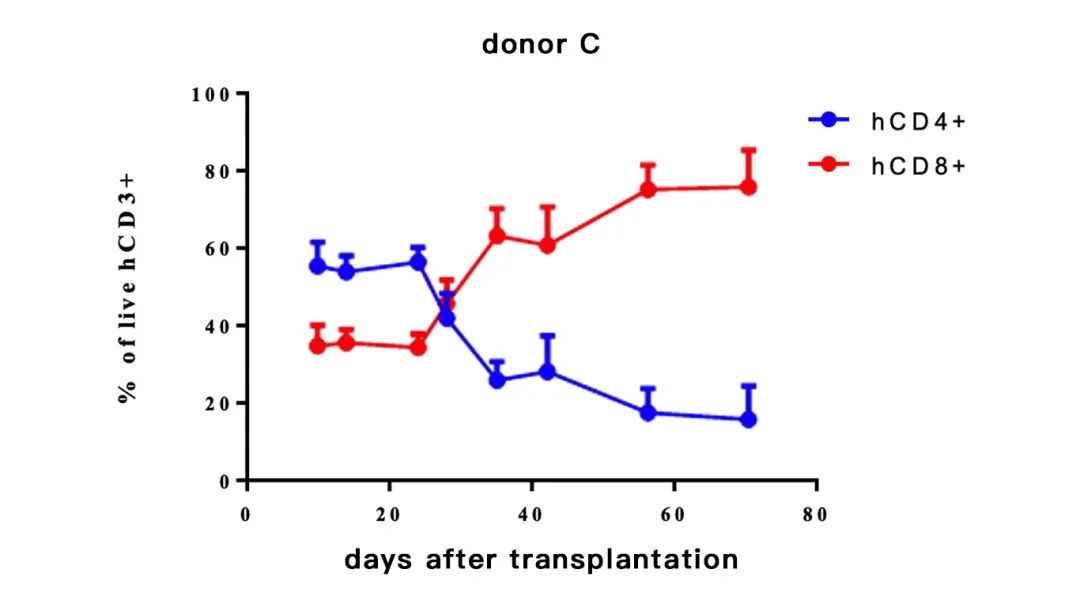
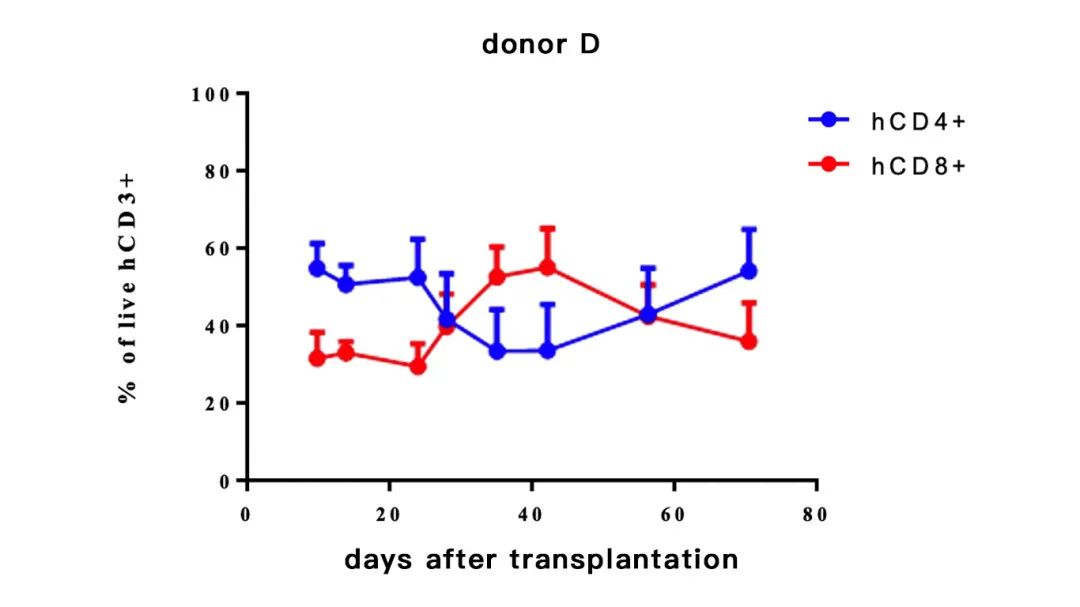
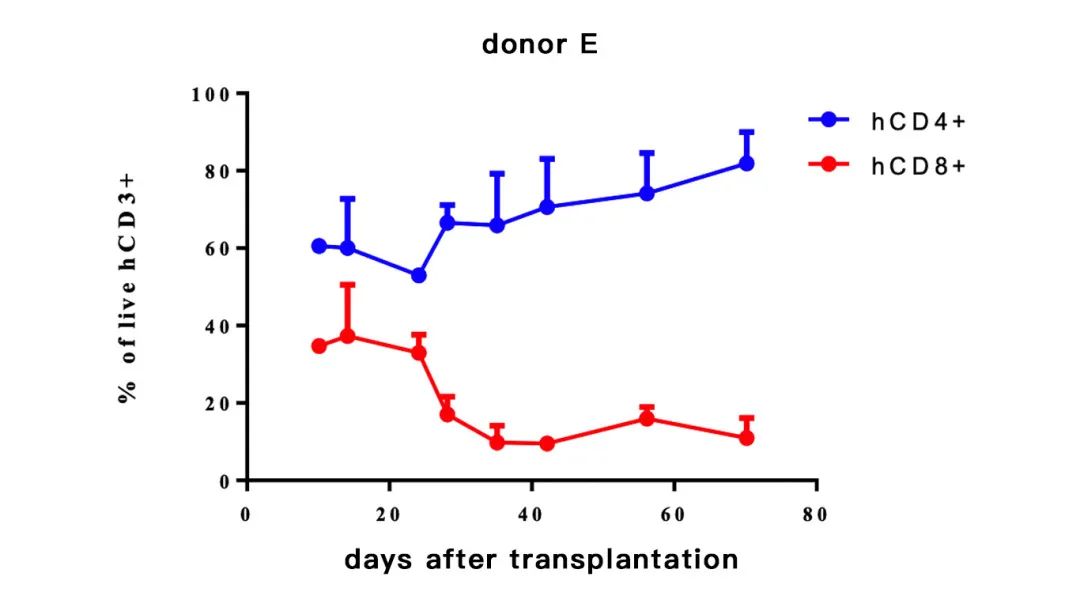
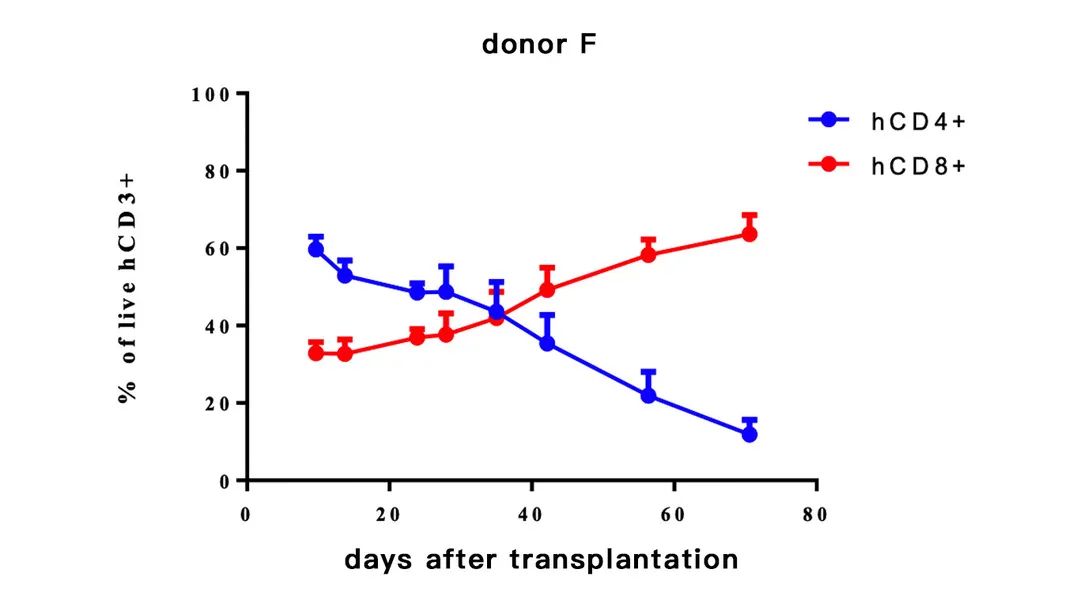
-不同供体来源的PBMC重建小鼠,hCD4(%)和hCD8(%)比例随着时间的变化会有不同; 研发者可根据自己的需求进行选择
维通利华人源化小鼠信息


1.Komatsu, Si., Kayukawa, Y., Miyazaki, Y. et al. Determination of starting dose of the T cell-redirecting bispecific antibody ERY974 targeting glypican-3 in first-in-human clinical trial. Sci Rep 12, 12312 (2022)
2.Galon J, Bruni D. Approaches to treat immune hot, altered and cold tumours with combination immunotherapies. Nat Rev Drug Discov. 2019 Mar;18(3):197-218
3.Yuan-Tong Liu, Zhi-Jun Sun. Turning cold tumors into hot tumors by improving T-cell infiltration. Theranostics. 2021 Mar 11;11(11):5365-5386




