作者:张利桃,Charles River 维通利华 产品经理,lynn.zhang@criver.cn
在肿瘤机制研究、免疫治疗开发、干细胞移植等前沿领域,对于huHSC免疫系统重建模型,维通利华之前给研发者提供了以下两种方案:
选择一:huHSC-NOG模型——需辐照、重建周期久、重建率和成功率相对较低,重建人源T/B细胞为主,且对HSC供体要求苛刻!
选择二:新一代人源化模型huHSC-NOG-EXL——重建率高、可重建多种免疫细胞、更模拟人免疫系统组成、更贴近临床,且比同类产品生存期更长!这是huHSC人源化模型的最优选,但由其成本相对较高使得部分研究人员望而却步!
本次全新升级的NOG-W41小鼠,以“超重度免疫缺陷+c-kit基因突变” 为核心优势,具有不需辐照,重建率高,不依赖供体,能重建人的红细胞和血小板等优势,是制备huHSC人源化模型的强势候补,同时在一些血液瘤模型制备上优势突出,可助研发者突破实验瓶颈,抢占科研先机!
NOG-W41小鼠在NOG小鼠基础上通过用TALEN技术引入了c-Kit基因的V831M突变,特性如下:
✓ 具有NOG小鼠超重度免疫缺陷的表型:T/B/NK三重缺失;
✓ 具备因c-Kit基因突变引发的自发性贫血,小鼠本身造血干细胞功能受到抑制;
✓ 品系来源清晰,引种于全球第一款超重度免疫缺陷小鼠NOG的研发机构-日本CIEM;
✓ 严格按照SOP进行生产繁育,同时隔离包饲养保证动物健康状态免受病原微生物侵扰;
✓ 存活期长,30周龄动物存活率高达90%以上;
✓ 无需辐照即可移植huHSC进行免疫重建;
✓ 移植huHSC前若进行低剂量辐照,造模成功率更高,免疫重建效果更好;
✓ huHSC注射量少,节约实验成本,单一HSC供体可制备更多的人源化模型;
✓ 提高PDX模型植入成功率,特别是血液瘤造模;
✓ 肿瘤学研究:移植人源肿瘤细胞/肿瘤组织构建CDX/PDX模型、药效评估
✓ 免疫治疗:无需辐照即可移植huHSC进行免疫重建,用于靶点在T细胞上的肿瘤免疫治疗研究:特异性抗体、免疫检查点抑制剂和组合疗法等研究
✓ 地中海贫血研究
✓ 感染与免疫:HIV/EBV等病毒感染机制研究
✓ 干细胞与再生医学:无需辐照即可移植人源造血干细胞或间充质干细胞并进行相关机制研究
NOG-W41小鼠注射huHSC前
是否进行辐照的免疫重建对比
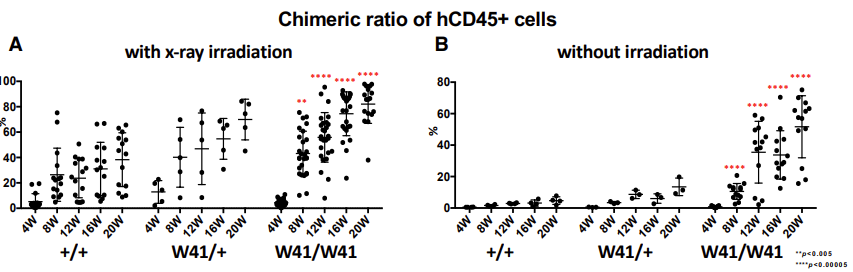
图1 NOG-W41小鼠移植huHSC前不进行辐照处理即可免疫重建成功,若进行辐照处理则重建效果更好!
NOG-W41和NOG同时移植低质量的
hCD34+细胞供体进行免疫重建对比
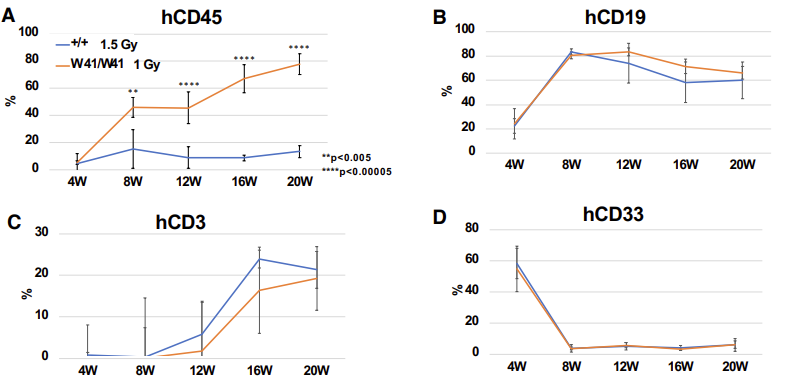
图2 低质量的hCD34+细胞供体在NOG小鼠中的hCD45+细胞嵌合率低于20%,而在NOG-W41小鼠中表现出较高的嵌合率,进一步证实NOG-W41对HSC供体具有更高的兼容性。
NOG-W41小鼠生存曲线
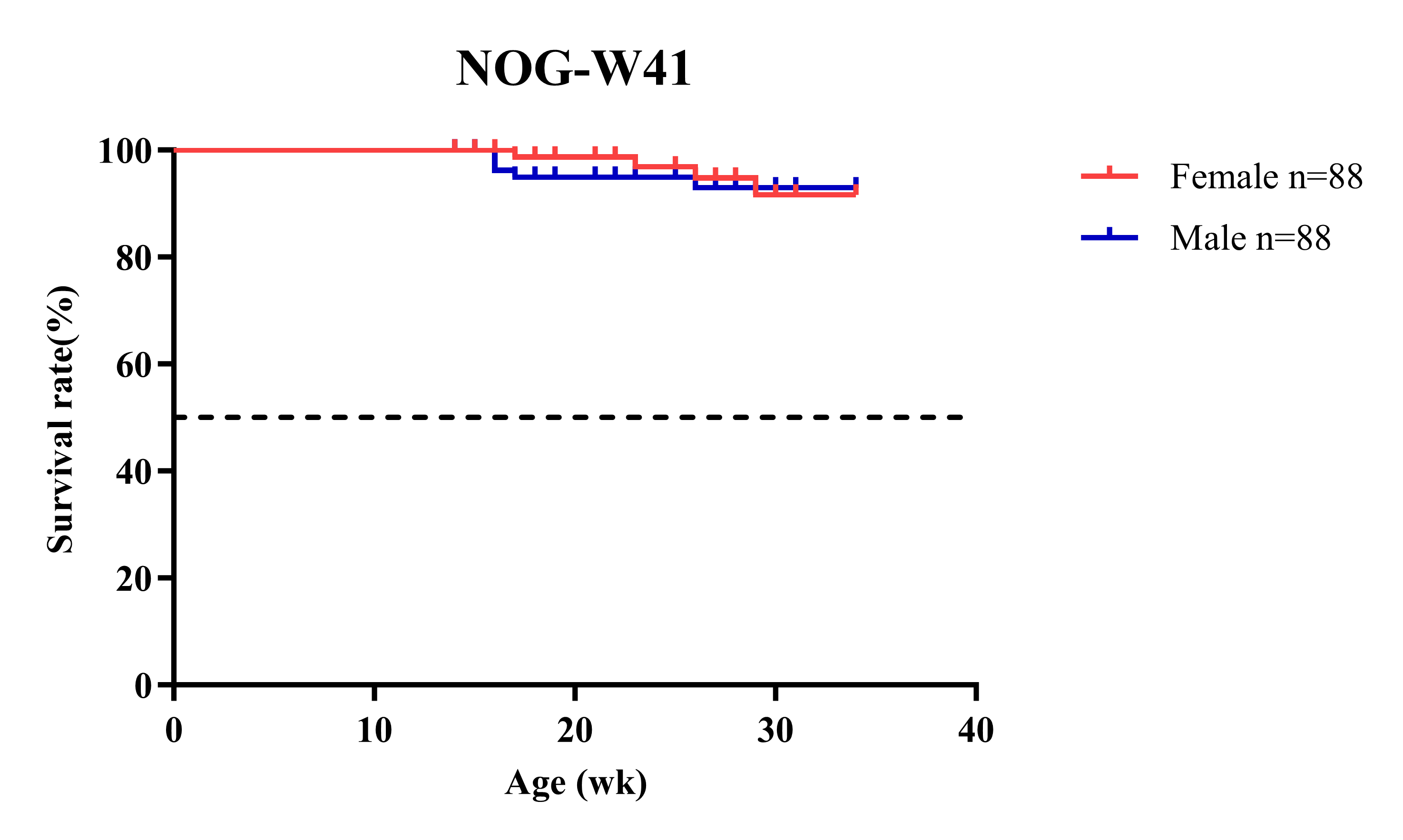
图3 NOG-W41小鼠生存期长,雌性或雄性30周龄的小鼠存活率均可达90%以上。
huHSC-NOG-W41模型外周血免疫重建水平
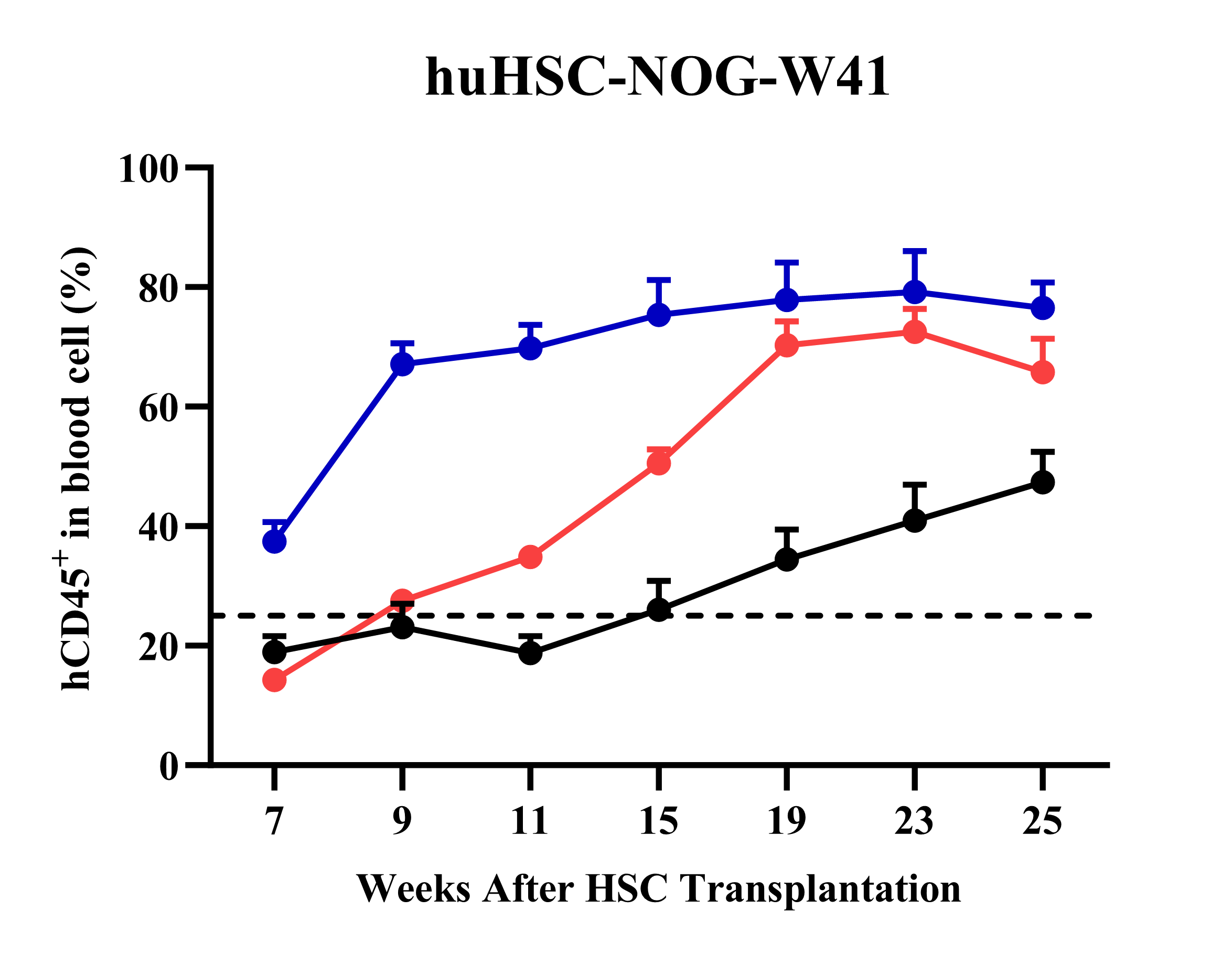
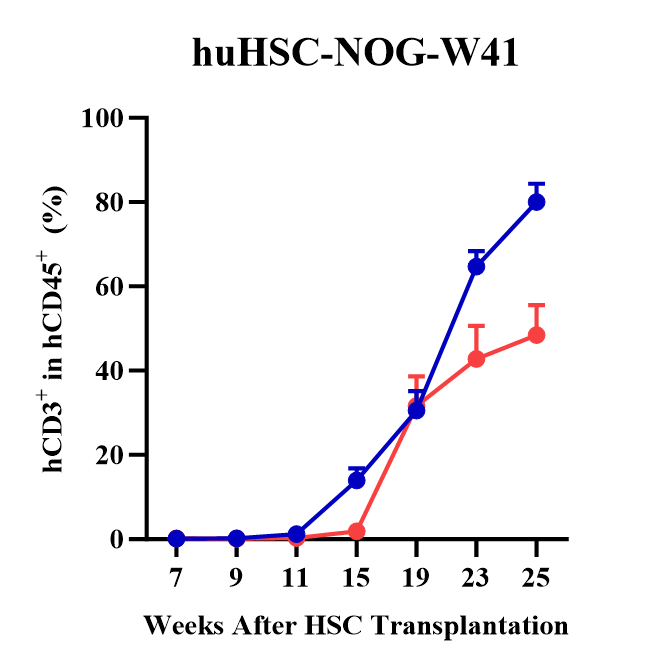

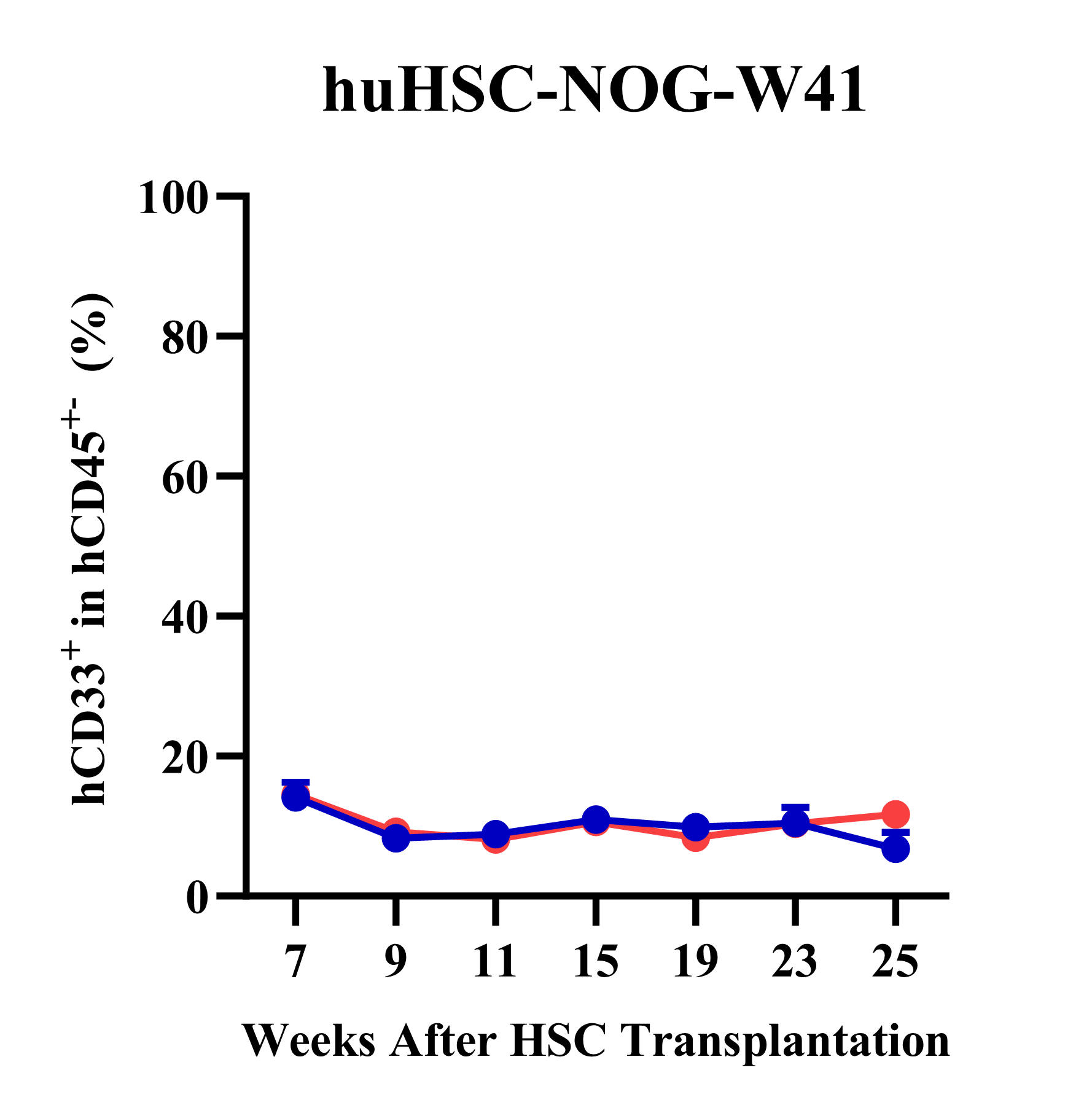
图4 与辐照后的NOG小鼠相比,NOG-W41小鼠移植huHSC后虽同样主要重建人源T、B细胞,但免疫重建水平更高。如果在huHSC移植前进行低剂量辐照,则可加速免疫重建进程。
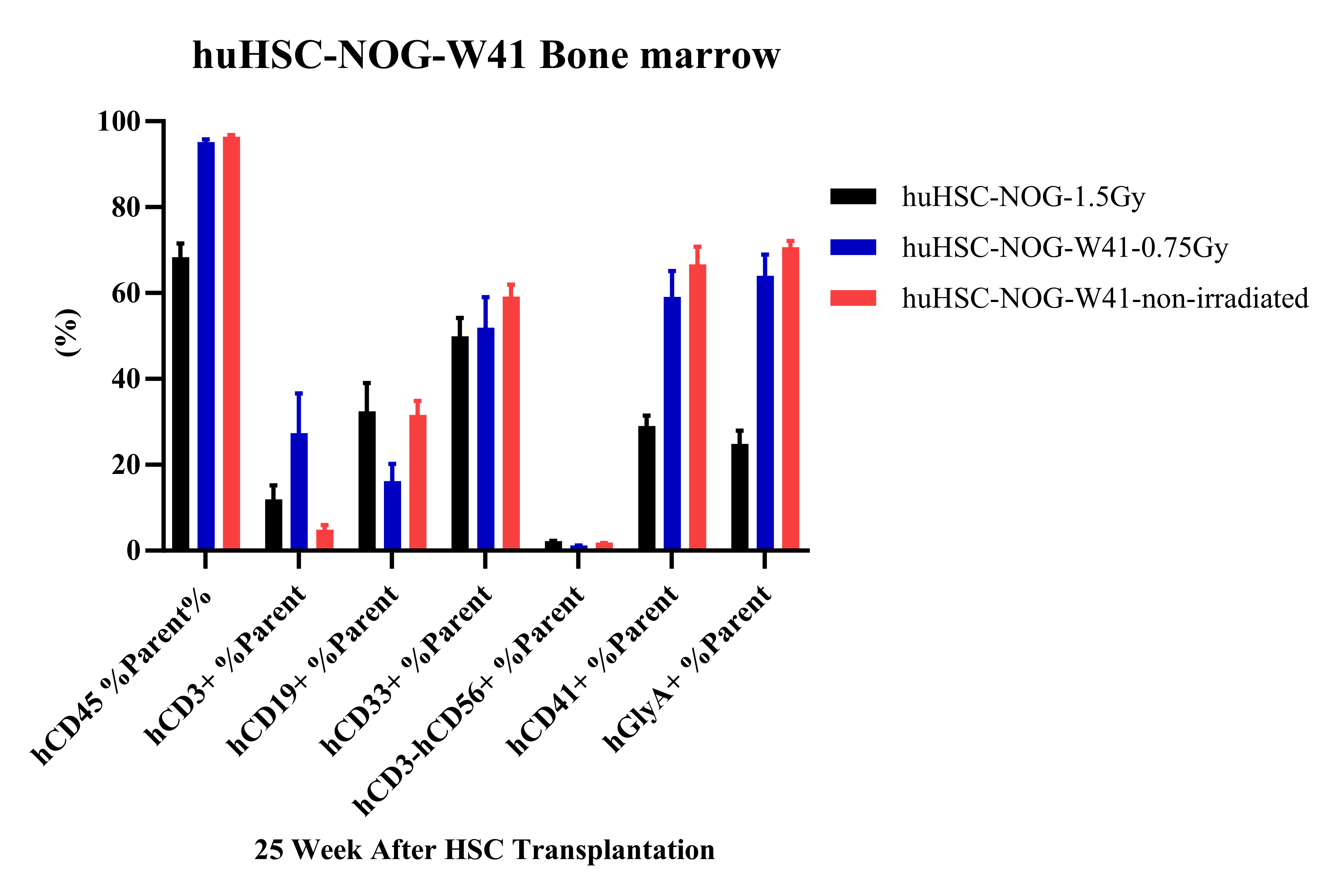
图5 huHSC移植后,骨髓中主要重建人源T、B及髓系细胞。但与辐照后的huHSC-NOG相比,huHSC-NOG-W41不论前期是否进行辐照,免疫重建水平以及骨髓中人源血小板和红细胞重建水平都显著更高。
huHSC-NOG-W41模型体重变化趋势
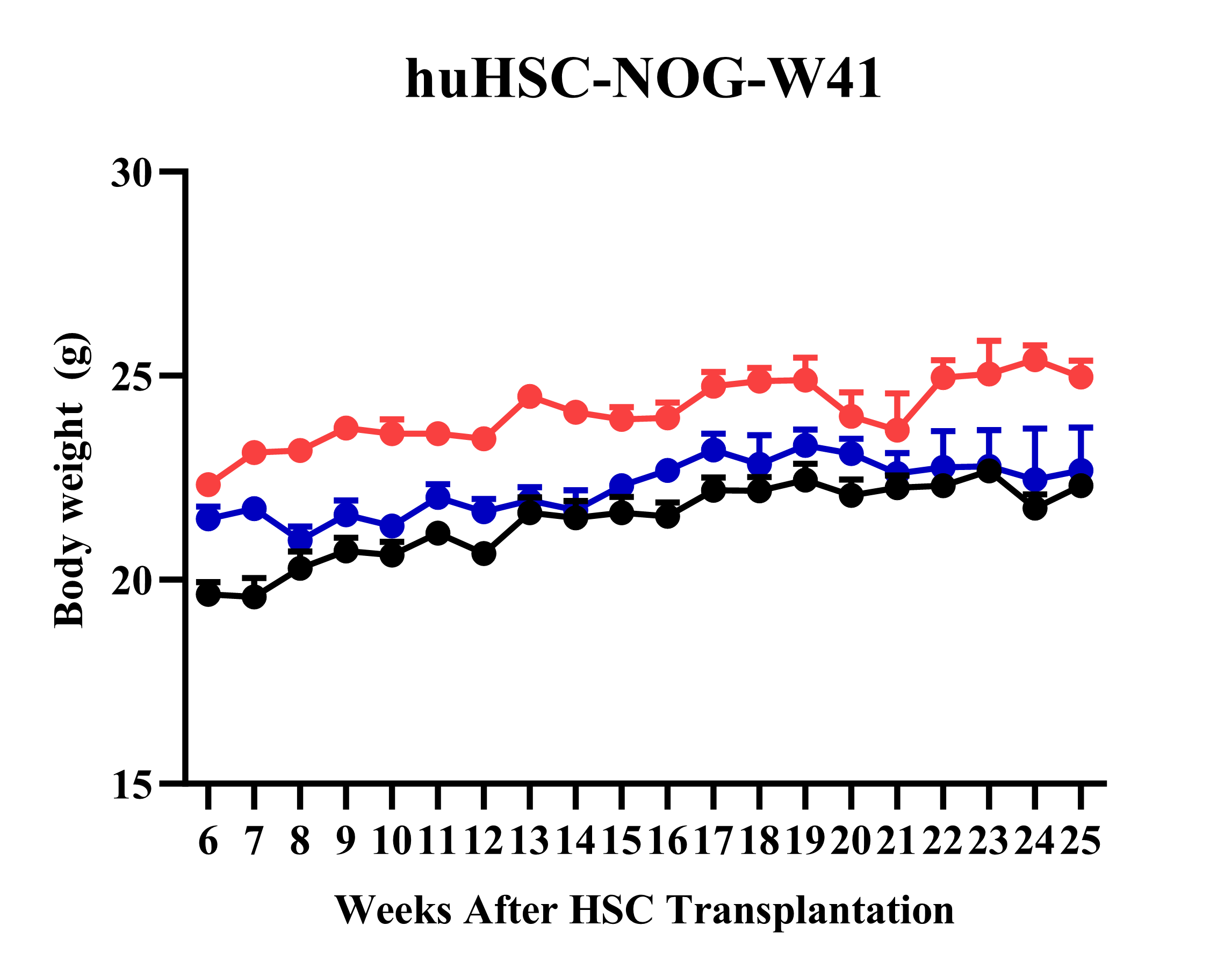

图6 不论huHSC移植前是否进行辐照处理,huHSC-NOG-W41模型体重都在稳定增加,且未经辐照处理的动物体重增长更快。
2023年,Hiromitsu Nakauchi教授带领团队在《Nature》上发表文章,建立了一种支持造血干细胞在体外长期扩增的新型培养系统,并将体外扩增培养好的造血干细胞回输到NOG和NOG-W41小鼠体内进行免疫重建实验以验证干细胞的活性 [1]。
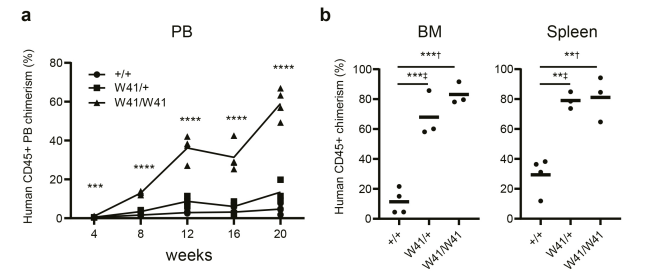
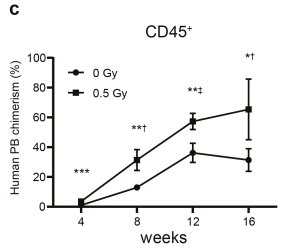
图7 与NOG(+/+)或NOG(W41/+)相比,将经体外扩增培养的造血干细胞移植到NOG-W41小鼠体内可以实现更高水平的免疫重建。如图7c所示,若NOG-W41移植HSC前进行低剂量辐照,免疫重建效果更好。
使用NOG-W41小鼠进行血液瘤PDX造模,可以省去辐照这一流程,节约实验成本的同时规避因辐照仪器不稳定而引发的风险,造模稳定性大幅提升!
无论您是深耕肿瘤机制、开发新型免疫疗法,还是挑战再生医学难题,NOG-W41小鼠 都将以其以其“超重度免疫缺陷+c-kit基因突变”的核心优势成为强势候补模型!
立即行动,让NOG-W41成为您下一个重磅成果的起点!
我们可以提供如下服务:
产品咨询:Product@criver.cn
订购电话:010-84744555
订购邮箱:Order@criver.cn
[1] Masatoshi Sakurai et al. Chemically defined cytokine-free expansion of human haematopoietic stem cells. Nature, 2023, doi:10.1038/s41586-023-05739-9.




